Ciencia de las plantas
Fluctuación poblacional, hospederos, fecundidad y ciclo de vida del pulgón amarillo [Melanaphis sacchari (Zehntner)] en sorgo [Sorghum bicolor L. Moench] en Nicaragua
Population fluctuation, hosts, fecundity and life cycle of the yellow aphid [Melanaphis sacchari (Zehntner)] in sorghum [Sorghum bicolor L. Moench] in Nicaragua
La Calera
Universidad Nacional Agraria, Nicaragua
ISSN: 1998-7846
ISSN-e: 1998-8850
Periodicidad: Semestral
vol. 20, núm. 35, 2020
Recepción: 28 Febrero 2020
Aprobación: 14 Octubre 2020

Resumen: El sorgo (Sorghum bicolor), pertenece a la familia de las Poaceae, es producido por pequeños y medianos productores en Nicaragua; en 2016 fue atacado por el pulgón amarillo del sorgo (Melanaphis Sacchari Zehntner) una plaga recién introducida al país, en ese mismo año ocasionó pérdidas entre 30 y 40 %. Este estudio se realizó con el objetivo de determinar el comportamiento biológico y ecológico de Melanaphis sacchari Zehntner en el cultivo del Sorgo. Se llevó a cabo entre los meses de Julio a octubre del 2017, en el Centro Experimental El Plantel, donde se delimitó un ensayo de 36 m X 24.8 m, colocando seis trampas de dos colores (amarilla y roja), a tres diferentes alturas (0.5 m, 1.0 m y 1.50 m) en cada uno de los cuatro lados de la parcela obteniendo un total de 24 trampas, se realizaron muestreo de malezas gramíneas para determinar los hospederos alternos del pulgón, tomando tres puntos a una distancia de cinco metros de la parcela en cada una de las coordenadas geográficas, así mismo 100 plantas de sorgo se muestrearon para determinar la fluctuación poblacional del pulgón amarillo y sus enemigos naturales. Los resultados indicaron que las trampas de color amarillo son las que atraparon más insectos y vuelan indistintamente a las diferentes alturas evaluadas. Los principales enemigos naturales asociados al pulgón amarillo del sorgo encontrados son: especies de la familia Syrphidae, Chrysoperla externa, Cycloneda sanguínea y Ceraochrysa sp. La maleza hospedera predominante fue Sorghum halepense. Se presentaron grandes poblaciones de M. sacchari a los 72 días después de la siembra. M. sacchari alcanzó una fecundidad diaria de uno a 17 individuos por hembra con una progenie total de 63 a 86 ninfas pasando por cinco estadios ninfales, todo su ciclo de vida dura de 22 a 24 días.
Palabras clave: Fluctuación poblacional, hospederos alternos, trampas.
Abstract: Sorghum (Sorghum bicolor) belongs to the Poaceae family, produced by small and medium producers in Nicaragua; in 2016 it was attacked by the sugarcane aphid (Melanaphis Sacchari Zehntner), a recently introduced pest to the country, in this same year it caused losses between 30 and 40%. This study was carried out with the objective of determining the biological and ecological behavior of the sugarcane aphid in the cultivation of Sorghum. It was carried out between the months of July to October 2017, at the El Plantel Experimental Center, where a test of 36 m X 24.8 m was delimited, placing six traps of two colors (yellow and red), at three different heights (0.5 m, 1.0 m and 1.50 m) on each of the four sides of the plot obtaining a total of 24 traps, weed weeds were sampled to determine the alternate hosts of the aphid, taking three points at a distance of five meters from the plot In each of the geographic coordinates, likewise 100 sorghum plants were sampled to determine the population fluctuation of the yellow aphid and its natural enemies. The results indicated that the yellow traps are the ones that caught the most insects and fly indistinctly at the different heights evaluated. The main natural enemies associated with the yellow sorghum aphid found are: species of the Syrphidae family, Chrysoperla externa, Cycloneda sangunea and Ceraochrysa sp. The predominant host weed was Sorghum halepense. Large populations of M. sacchari appeared at 72 days after planting. M. sacchari reached a daily fecundity of one to 17 individuals per female with a total progeny of 63 to 86 nymphs which go through five nymphal stages, their entire life cycle lasts from 22 to 24 days.
Keywords: Population fluctuation, alternate hosts, traps.
Los sorgos se originaron del silvestre Sorghum bicolor sub especie Arundinaceum y la mayor variación en el género Sorghum se encuentra en el cuadrante noreste de África, abajo del Sahara, en la región de Etiopia-Sudan, donde probablemente se originó hace 5,000 a 6,000 años (Doggett, 1988; Snowden, 1955; Harlan y Wet, 1972)
El sorgo (Sorghum bicolor), perteneciente a la familia de las Poaceae, ocupando el quinto lugar en importancia entre los cereales del mundo después del trigo (Triticum aestivum L.), el maíz (Zea mays L.), el arroz (Oryza sativa L.) y la cebada (Hordeum vulgare L.) (Martin, 1985).
En Nicaragua el sorgo es producido por pequeños y medianos productores que lo utilizan para alimentación humana y animal: vacunos, cerdos y aves, siendo la parte utilizada el grano, forraje y/o rastrojo (Instituto Nicaragüense de Tecnología Agropecuaria [INTA], 2009). La producción de sorgo la destinan en gran parte al mercado local y el resto para autoconsumo y la alimentación de aves de patio, cerdos y para la siembra del siguiente ciclo productivo. El residuo de la cosecha (guate) es recogido, almacenado y utilizado en periodos secos para la alimentación del ganado bovino (Suarez y Zeledón, 2003).
La planta de sorgo se adapta a una amplia gama de ambientes y produce granos bajo condiciones desfavorables para la mayoría de los otros cereales. Debido a su resistencia a la sequía, se considera el cultivo más apto para las regiones áridas con lluvias erráticas (Purseglove, 1972).
La producción de sorgo en Nicaragua ha sido importante a lo largo del tiempo, este cultivo ha permitido a las familias nicaragüenses la obtención de ingresos y en ciertos casos asegurar la alimentación de las personas, también del ganado mayor y menor que poseen algunas familias del sector rural.
En Nicaragua se siembra anualmente unas 35 000 manzanas de sorgo, y su problemática es muy variada, va desde el acceso al crédito, los insumos, el cambio climático y las variedades disponibles. Aunque los productores siempre mencionan que las plagas (insectos, patógenos, malezas) son una de las principales limitantes en este cultivo (INTA, 2009).
M. sacchari es originario de África y medio Oriente. Actualmente está distribuido en todos los continentes excepto Antártida (Servicio Nacional de Sanidad, Inocuidad y Calidad Agroalimentaria [SENASICA], 2014). Los insectos adultos de M. sacchari, son de 1.6-2.0 mm, decoloración variable, dependiendo de la planta hospedera. Los adultos pueden ser alados o ápteros, tienen marcas dorsales escleróticas oscuras (Blackman y Eastop, 2000). M. sacchari se reproduce partenogenéticamente en forma vivípara dando origen a sólo hembras, pero en México y específicamente en Sinaloa, también presenta reproducción sexual, con presencia de machos.
El pulgón amarillo del sorgo apareció como una plaga emergente en el ciclo de postrera 2016, aunque se desconoce cómo y por dónde entró al país, y cómo tan fácilmente se desarrolló e hizo tantos estragos al cultivo en el año 2016. Las pérdidas ocasionadas por esta plaga se estiman en 10 millones de dólares, lo que significó un decrecimiento en la producción del cultivo en 300,000 quintales, y un daño en un área sembrada de 22 000 manzanas, ésta especie de insectos fue capaz de reducir los rendimientos comerciales de sorgo a nivel nacional entre 35 % y 40 % (Baca, 2017). Por esta razón se realizó este estudio con el objetivo de generar información nacional de la fluctuación poblacional, hospederos, la fecundidad y el ciclo de vida del pulgón amarillo del sorgo.
En Nicaragua esta plaga esta recién introducida y debido a que causa mucho daño a la producción de sorgo se hace necesario investigar su comportamiento ecológico y biológico para valorar posibles enemigos naturales y plantas hospederas, con ello brindar información pertinente a nivel nacional.
MATERIALES Y MÉTODOS
El estudio se realizó de julio a diciembre del 2017 en el centro experimental El Plantel, propiedad de la Universidad Nacional Agraria, localizado en el kilómetro 30 Carretera, Tipitapa-Masaya. Corresponde a una zona que se considera un bosque seco tropical, entre las coordenadas geográficas 12°06´24” de Latitud Norte y los 86°04´06” de Longitud Oeste. A una altura de 65 metros sobre el nivel del mar (msnm), con temperatura promedio de 28 °C, las precipitaciones promedio anual oscila entre los 796-800 mm, con humedad relativa de 71 % y viento con velocidad de 3.5 m s-1 (Instituto Nicaragüense de Estudios Territoriales [INETER], 2009).
El estudio es una investigación combinada que tiene una parte experimental donde se estudió el efecto que puede tener el color de las trampas y las alturas de las mismas (0.5 m, 1.0 m, 1.5 m) para determinar la altura de vuelo de M. sacchari y por cuál de los colores es más atraído. Los puntos de muestreos realizaron una función de agrupación por bloque utilizando el Modelo Aditivo Lineal ajustado y la parte no experimental a través del seguimiento al ciclo de vida que se determinó mediante el método observacional del insecto. También como otra bajo este mismo método se describió el comportamiento de la fauna insectil benéfica asociadas al cultivo de sorgo.
Para la realización del estudio se estableció un área de 892.8 metros cuadrados de sorgo granífero [Sorghum bicolor (L) Moench], sembrados a un metro entre surco y a chorrillo, cada surco de 36 metros de largo. Asimismo, en los alrededores del área donde se estableció el cultivo de sorgo se colocaron las trampas a un metro de distancia del cultivo y a diferentes distancias según los puntos de muestreo entre trampas de colores, considerando los lados norte, este, sur y oeste como los cuatro puntos asignados.
Una vez definidos estos puntos se colocaron trampas de plástico horizontales de color amarilla y roja, a tres alturas de 0.5 m, 1.0 m y 1.5m para un total de seis trampas por punto cabe mencionar que estas eran impregnadas con Zapicol® mezclado en diluyente con una relación de uno a uno como atrayente para los insectos.
De igual manera ocho días después de la siembra se realizaron muestreos en los cuatro sitios seleccionados dentro del área del cultivo,y quedaron distribuidos de una forma representativa, en cada sitio se seleccionaron 25 plantas al azar, teniendo un total de 100 plantas, las cuales fueron muestreadas de forma estratificada. La frecuencia de muestreofue cada ocho días, en las 25 plantas/sitio, se realizaron recuentos de áfidos alados, áfidos ápteros, colonias de áfidos y cantidades de enemigos naturales por planta.
Para la identificación de las principales gramíneas hospederas del pulgón amarillo se seleccionaron 3 puntos, en un área de cinco metros alrededor del cultivo, considerando los lados norte, sur, y este como los sitios de muestreo.
El ciclo de vida para M. sacchari se realizó mediante el establecimiento de dos variedades de sorgo, Tortillero e INTA CENIA en maceteras de plástico de 10 cm de diámetro y 12 cm de alto, las cuales fueron ubicadas en jaulas con una criba de 50 um, como medida de protección para las plantas que estaban dentro cuyo tamaño era de 1.50 m de alto y 50 cm de ancho. Se establecieron nueve plantas para cada variedad, las cuales fueron separadas en grupos de tres y ubicadas en jaula teniendo un total de seis jaulas y 18 plantas. Se colocaron dos trampas clic por planta de cuatro centímetros de diámetro y ocho centímetros de largo, estas fueron infestadas con un adulto de M. sacchari, los cuales dieron origen a crías en poco tiempo. De este modo se seleccionó una ninfa por trampa teniendo un total de 36 individuos. En estas se observó la duración de cada uno de sus estudios hasta llegar adulto, se determinó la reproductividad y la duración de su ciclo de vida.
El muestreo de los insectos se realizó una vez por semana, utilizando trampas pegajosas amarillas y rojas a tres alturas (0.50 m, 1.0 m, 1.50 m) alrededor de la parcela. Estas se colocaron a un metro de distancia en la periferia del cultivo, ubicándose los puntos este y oeste a una distancia de tres metros entre trampas y en los puntos norte y sur a una distancia de cinco metros. Se determinó la altura de vuelo y preferencia por el color (amarillo o rojo). Estas se cambiaron semanalmente.
El método de los cuadrantes se utilizó para ver los hospederos de M. sacchari, en un área perimetral de cinco metros alrededor de la parcela. En cada uno de los lados del área experimental se tomaron al azar tres puntos en los cuales se identificaron los arvenses (gramíneas) con síntomas, signos o presencia de M. sacchari.
Para determinar el ciclo de vida se realizó la siembra de semillas de sorgo en macetas plásticas previamente desinfectadas con cloro al 10 %m, posteriormente a los 26 días después de emergidas las plantas se procedió a colocar dos trampas clic. Las hojas fueron infestadas con un adulto de M. sacchari. Después de un lapso de cuatro horas todos los adultos dieron origen a varias ninfas lasque en su mayoría incluyendo al adulto fueron descartadas dejando un solo insecto en estado ninfal. En esta ninfa se observó el tiempo que transcurre desde la aparición de su primer estadio ninfal hasta llegar a adulto, posterior a eso se contabilizaron el número de ninfas que dieron origen los adultos ápteros por día, hasta la finalización de su ciclo reproductivo.
Las variables evaluadas fueron: preferencia de altura de vuelo de M. sacchari , número de áfidos ápteros/planta, número de áfidos alados/planta, número de colonia de áfidos/planta, número de huevos de C. sanguínea , número de larvas de C. sanguínea , número de C. sanguínea/Planta , número de adultos de araneae/planta, número de huevos de C. externa /planta , número de larvas de C. externa /planta , número de adultos de C. externa /planta , fluctuación poblacional de insectos , gramíneas hospederos de M. sacchari , duración en días de su primer estadio ninfal hasta llegar a su estado adulta, reproductividad y duración del ciclo de vida.
Una vez colectados todos los datos en campo, fueron agrupados en tablas de Excel por variables para su posterior análisis estadístico utilizando el programa SAS (Statistical Analysis System por sus siglas en inglés [SAS], 2002). Con un nivel de confianza del 95%. Se hizo una transformación de raíz cuadrada + 0.5 y una transformación de Log10 + 1, con el objetivo de obtener una mejor normalización de los datos debido a que el comportamiento de los insectos es anormal lo que provoca mucha variabilidad en cuanto a la captura de los insectos. Se realizó un análisis de varianza para ver efectos de trampas por altura, color y fechas de muestreos posteriormente se realizó pruebas de comparación de medias Tukey (<0.05) para evidenciar a que variable se le atribuye el efecto significativo.
RESULTADOS Y DISCUSIÓN
Altura de vuelo y color de preferencia para M. sacchari.
La comparación de medias con la prueba de Tukey, demostró que existió efecto significativo (p< 0.0001) en la captura de M. sacchari según color de trampa predominando el amarillo con un promedio de 13.65 en comparación al rojo con 0.82 (Cuadro 1), lo que significa que el color es determinante en la atracción de este insecto en lo que corresponde a propósitos de monitoreo y no así la altura de vuelo evaluada en este estudio. Bravo-Portocarrero et al., 2020 reportan que pulgones son eficientemente atraídos por trampas amarillas en 26% y con trampas verdes en un 20%, por otro lado Trampas pegantes de colores se han venido utilizando para investigar su eficiencia en la captura de insectos (Gharekhani et al., 2014; Böckmann y Meyhöfer, 2017; Tarwotjo et al., 2019; Pobozniak et al., 2020).
| Familia | M. sacchari | D. maidis | C. sanguínea | C. externa | Syrphidae |
| Trampa | Medias | Medias | Medias | Medias | Medias |
| Amarillo | 13.65 a | 53.94 a | 0.43 a | 0.07 a | 1.03 a |
| Rojo | 0.82 b | 13.52 b | 0.11 b | 0.07 a | 0.35 b |
| Altura (Metro) | Medias | Medias | Medias | Medias | Medias |
| 0.5 | 8.49 a | 57.49 a | 0.32 a | 0.05 a | 0.90 a |
| 1.0 | 6.42 a | 26.76 b | 0.37 a | 0.11 a | 0.63 a |
| 1.5 | 5.07 a | 16.07 b | 0.12 a | 0.05 a | 0.56 a |
Medias con igual letra no difieren estadísticamente (Tukey, α=0.05).
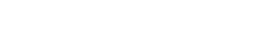
Fluctuación poblacional de alados y ápteros de M. sacchari con relación a la fenología del cultivo de sorgo.
Las poblaciones de alados y ápteros de este insecto se presentaron en todas las etapas de muestreo (Figura 1), pero a partir de los 72 días después de la siembra (dds) las poblaciones de pulgones ápteros aumentaron de forma progresiva a través del tiempo manteniendo su nivel poblacional siempre por encima de los niveles críticos. Esto se encuentra relacionado a la etapa fenológica del cultivo (Específicamente la fase reproductiva) donde es más susceptible al daño por este insecto y que junto con la temperatura como elemento climatológico son los que más influyen en el desarrollo del M. sacchari (SENASICA, 2014)
Según Chang et al. (1982), el estado fenológico de cultivo tiene un efecto significativo en el crecimiento de la población y se desarrolla más en toda la etapa vegetativa y parte de la reproductiva además de que la temperatura favorece la dispersión, La densidad de población de los insectos se ve afectada por la temperatura y los patrones de lluvia.
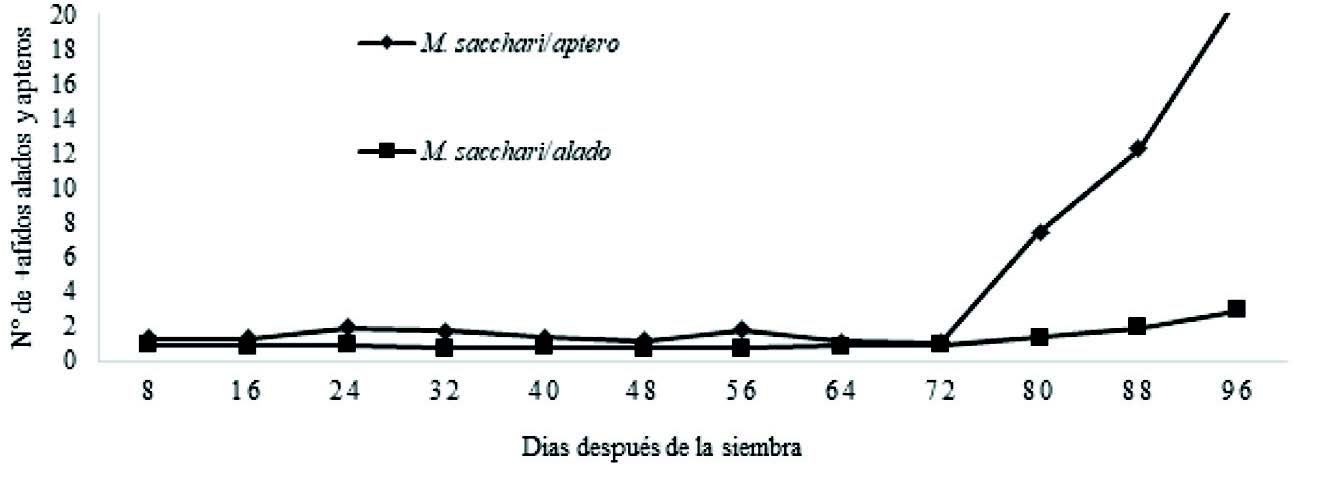
Fluctuación poblacional de los enemigos naturales de M.sacchari con relación a la fenología del cultivo.
Se midió la fluctuación poblacional de agentes de control biológico en los diferentes días de muestreo (Figura 2) se observó que las poblaciones de enemigos naturales se encontraron en todas las etapas de muestreo que se realizaron en todas las etapas fenológicas del cultivo, los mayores picos poblacionales se presentaron en los días 32, 56 y 96 después de la siembra para el caso de depredadores como araña 80, 88 y 96 días después de la siembra para Syrphidae, presentando además las mayores poblaciones, por otro lado C. sanguínea, C. externa y Ceraochrysa sp. mantuvieron sus poblaciones en equilibrio para todas las fechas de muestreo.
La población de enemigos naturales tiene un gran efecto sobre las poblaciones de M. sacchari como se puede observar en la Figura 2. Las poblaciones de áfidos aumentan a partir del día 72 después de la siembra por lo tanto hasta tal fecha tiene un efecto sobre dicha plaga.
Quijano-Carranza et al. (2017), registra como fauna benéfica numerosos organismos, entre estos: C. sanguínea, C externa y Ceraochrysa sp. Que consumen grandes cantidades de ninfas de áfido y otros de los que mencionan son los sirfidos y las arañas los que coinciden con los encontrados en esta investigación.
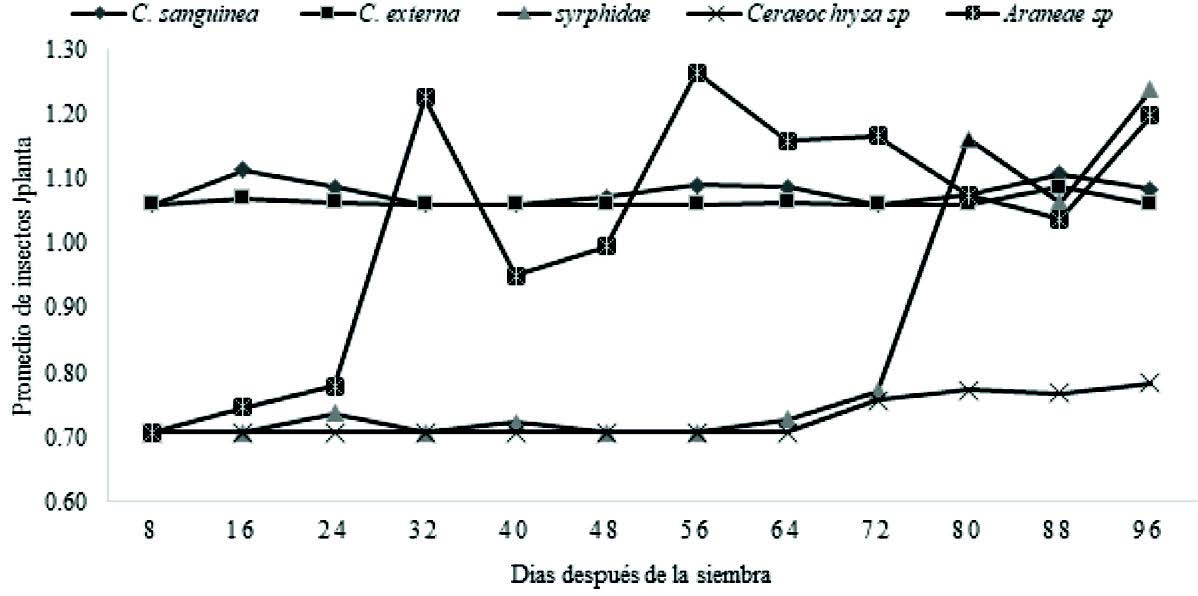
Hospederos alternos de M. sacchari.
Según Rodríguez y Hernández (2014), todos los hospederos de los cuales se alimenta, reproducen y hospeda (M. sacchari) pertenecen a las Poaceae, principalmente de la familia de las gramíneas. El sorgo se considera como su principal hospedero seguido de Arvenses como Sorghum halepense, como hospederos secundarios tenemos el maíz, trigo, cebada, entro otros.
Según los resultados se logró identificar 4 especies de hospederos: Shorgum halepense, Ixophorus unisetus, Zea mays, Rottboellia cochinchinensis.
Como se puede observar en el resultado obtenido en la Figura 3, de todas las fechas de muestreos el S. halepense fue el que obtuvo el mayor número de individuos con 1039, seguido de I. unisetus con 106 individuos, Z. mays con ocho y R. cochinchinsis con siete individuos, lo que coincide con estudios realizados por SENASICA (2014) que indican que el hospedero más importante de M. sacchari es S. halepense.
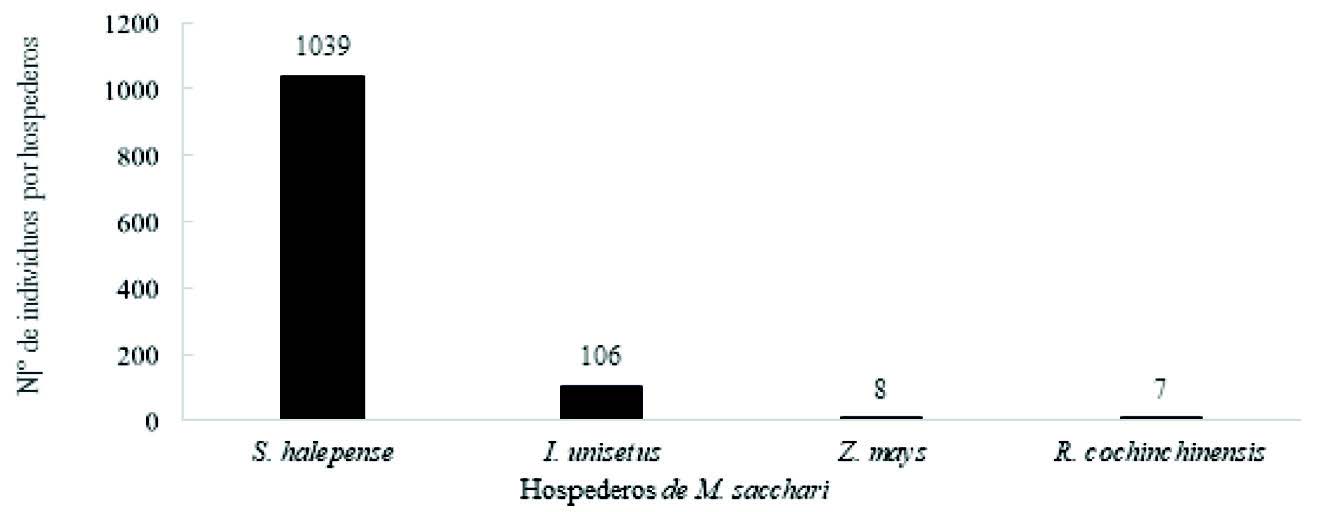
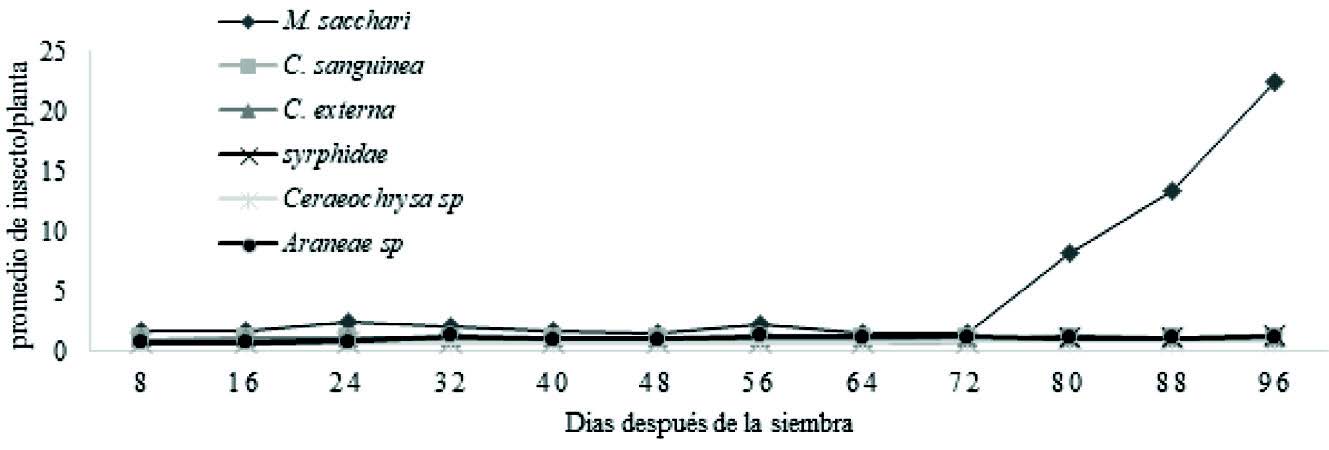
Fluctuación poblacional de M. sacchari y sus enemigos naturales en diferentes estados de su ciclo de vida con relación a la fenología del cultivo.
Se determinó la fluctuación de M.sacchari y la de sus agentes de control biológico en todas las etapas del estado fenológico del cultivo (Figura 4). Se observó que las poblaciones de M. sacchari se encontraron en todas las fechas de muestreo, los mayores picos poblacionales para M. sacchari se presentaron a los 72 dds, lo que significa un aumento después de la etapa vegetativa del cultivo, a diferencia de sus enemigos naturales que registraron sus mayores picos poblacionales a los 32, 56, y 96 dds.
El análisis de varianza para las fechas de muestreo, acerca del comportamiento de M.sacchari y a sus diferentes controladores biológicos (Cuadro 1) determinó que existe diferencia significativa entre fechas de muestreo (p = 0.0001) para áfidos, arañas y Syrphidae.
Por otro lado, la figura 4. muestra que los picos de población más bajos para los áfidos se presentaron a los 8 y 16 dds a diferencia de las arañas que fue a los ocho dds y Syrphidae que pasó desde los ocho dds hasta los 72 dds, aumentando después de la etapa vegetativa del cultivo al mismo tiempo que las poblaciones de pulgones comienzan a elevarse. Así mismo de esta manera se observó que las especies C. sanguínea, C. externa y Ceraeochrysa sp. se mantuvieron en contaste equilibrio durante todas las fechas de muestreos.
Duración de primer estadio ninfal hasta su etapa adulta de M. sacchari.
La duración del periodo de desarrollo M. sacchari fue de 5 días en promedio teniendo en cuenta las dos variedades (INTA CENIA y Tortillero) y las temperaturas que oscilaban entre los 26-28°C de acuerdo a las mediciones de las mismas en cada muestreo realizado.
El tiempo necesario para llegar adulto y completar una generación es muy corto, de acuerdo con Setokuchi, (1979) a 15°C tarda 10.9 días, a 20°C 7.3, a 25°C 5.2 y 30°C 3.5 días.
Según SENASICA (2014), el pulgón amarillo presenta cuatro estadios ninfales, los cuales se desarrollan en aproximadamente 5.4 días a 25 °C, lo que coincide con los resultados del presente estudio. Según Behura y Bohidar (1983), a temperaturas mayores de 35°C pueden presentarse altas mortalidades.
Fecundidad de M. sacchari.
Durante el período reproductivo la especie alcanzó una reproductividad diaria de 1 a 17 individuos por hembra compartidas en ambas variedades, teniendo en cuenta que no todos los días se llevaba a cabo el nacimiento de una nueva ninfa por adulto. Obteniendo así una progenie total de 63 a 86 ninfas teniendo en cuenta las temperaturas promedio °C y las variedades (INTA CENIA y Tortillero) que fueron utilizadas en el ensayo. Por cada una de las variedades se obtuvo un promedio de 83.8 ninfas para tortillero y 111.3 para la variedad INTA CENIA. Según Chang et al. (1982), ha reportado que bajo condiciones de cautiverio pueden desarrollarse de 51 a 61 generaciones en un año.
Según Rensburg (1973), debido al potencial de reproducción de M. sacchari, una sola planta puede ser atacada hasta por 30,000 áfidos. Los áfidos presentan un ciclo de vida complicado debido a las diversas estudios por las que pasan y a las formas que adoptan. Según la planta hospedante, pueden distinguirse distintos tipos: Monoecias y Heteroecias. Según la forma de reproducción pueden ser: Vivíparos y Ovíparos.
Este fitófago posee una longevidad de entre 17 a 19 días después de haber iniciado su proceso reproductivo y un ciclo de vida de 22 a 24 días tomando en cuenta las temperaturas promedio y las dos variedades de sorgo INTA CENIA y Tortillero.
Según Voegtlin et al. (2003) y David (1977), la reproducción de M. sacchari es predominantemente asexual, con hembras adultas ápteras y aladas. M. sacchari en su forma adulta es áptero y a veces alado, tienen marcas dorsales escleróticas de tonalidad oscuras. Es de color amarillo grisáceo, algunas veces de color marrón. Tienen una longitud de 1.4 mm. Las antenas generalmente con seis segmentos con una longitud un poco mayor a la mitad del cuerpo. El unguis o proceso terminal de la antena es cuatro veces la base del VI segmento antenal.
La cauda es oscura notoriamente constreñida y ligeramente más larga que los cornículos con cuatro setas a los lados. El estilete alcanza el segundo par de coxas. Los cornículos son oscuros cónicos adelgazados hacia el ápice, con reborde notorio, son cortos y miden aproximadamente la mitad de longitud del cuerpo. El margen frontal es liso (Bustillo y Sánchez, 1977). Las formas ápteras tienen 1.6 mm de largo, y un ancho de 0.6 mm mientras que los alados son un poco más grandes (Denmark, 1988).
CONCLUSIONES
M. sacchari vuela indistintamente a cualquiera de las alturas evaluadas de 0.5 m , 1.0 m y 1.5 m, además las trampas de color amarillo atraen más a M. sacchari en el cultivo de sorgo.
M. sacchari se presentó en todas las fechas de muestreo, coincidiendo su aumento significativo en la etapa reproductiva del cultivo que es cuando es más susceptible.
Los principales hospederos de Melanaphis sacchari son: Sorghum halepense, Ixophorus unisetus, Zea mays, Rottboellia cochinchinensis y la que más individuos hospedó fue Sorghum halepense seguido Ixophorus unisetus.
M. sacchari pasa por cuatro estadios ninfales en cinco días hasta llegar a ser adulto, con una duración del ciclo de vida de 22 a 24 días con una tasa reproductiva de de uno a 17 individuos por hembra por día con una progenie entre 63 y 86 en total.
Referencias
Baca, L. (2017). El sorgo está en peligro en Nicaragua. La Prensa. https://www.laprensa.com.ni/2017/02/25/economia/2188762-sorgo-esta-en-peligro-en-nicaragua
Behura, B. K., y Bohidar, K. (1983). Effect of temperature on the fecundity of five species of aphids. Pranikee, 4, 23-27.
Blackman, R. L., y Eastop, V. F. (2000). Aphids on the world's crops: an identification and information guide (2da ed.). John Wiley & Sons Ltd.
Böckmann, E., y Meyhöfer, R. (2017). Sticky trap monitoring of a pest-predator system in glasshouse tomato crops: are available trap colours sufficient?. Journal of Applied Entomology, 141(5), 339-351.
Bravo-Portocarrero, R., Zela-Uscamayta, K., y Lima-Medina, I. (2020). Eficiencia de trampas pegantes de colores en la captura de insectos de hortalizas de hoja. Scientia Agropecuaria, 11(1), 61-66. https://www.doi.org/10.17268/sci.agropecu.2020.01.07
Bustillo, A., y Sánchez, G. (1977). Los áfidos en Colombia: plagas que afectan los cultivos agrícolas de importancia económica.
Chang, C. P., Fang, M. N., y Tseng, H. Y. (1982). Studies on the life history and varietal resistance in grain sorghum aphid, Melanaphis sacchari Zehntner in central Taiwan. Chinese Journal of Entomology, 2, 70-81.
David, S.K. (1977). Host-selection and speciation in some south Indian Aphids. En Ananthakrishnan, T.N. (Ed.), Insects and host-specificity (pp. 19-21). The Macmillan Company of India Ltd.
Denmark, H.A. (1988). Surgacane aphids in Florida. (Homoptera: Aphididae). Entomology Circular, 302. https://www.fdacs.gov/content/download/10694/file/ent302.pdf
Doggett, H. (1988). Sorghum (2da ed.). Longman.
Gharekhani, G.H., Ghorbansyahi, S., Saber, M. y Bagheri, M. (2014). Influence of the colour and height of sticky traps in attraction of Thrips tabaci (Lindeman) (Thysanoptera, Thripidae) and predatory thrips of family Aeolothripidae on garlic, onion and tomato crops. Archives of Phytopathology and Plant Protection, 47(18), 2270-2275.
Harlan, J.R., y de Wet, J.M.J. (1972). A Simplified Classification of Cultivated Sorghum. Crop Science, 12 (2), 172-176.
Instituto Nicaragüense de Estudios Territoriales (INETER). (2009). Promedios de Temperatura (°C), Precipitación (mm) y Humedad relativa (HR %) en El Centro Experimental El Plantel, Tipitapa.
Instituto Nicaragüense de Tecnología Agropecuaria. (2009). Guía técnica del sorgo (2da ed.).
Martin, F.W. (1985). Sorghum. En CRC Handbook of Tropical food crops. CRC press, Inc.
Pobozniak, M., Tokarz, K., y Musynov, K. (2020). Evaluation of sticky trap colour for thrips (Thysanoptera) monitoring in pea crops (Pisum sativum L.). Journal of Plant Diseases and Protection, 127, 307-321. https://doi.org/10.1007/s41348-020-00301-5
Purseglove, J. W. (1972). Tropical crops. I. Monocotyledons. John Wiley.
Quijano-Carranza, J. A., Pecina-Quintero, V., Bujanos-Muñiz, R., Marín-Jarillo, A., y Yáñez-López, R. (2017). Guía 2017 para el manejo del pulgón amarillo del sorgo. INIFAP.
Rensburg, N.J.V., (1973). Notes on the occurrence and biology of the sorghum aphid in South Africa. Journal of the Entomological Society, 36(2), 293-298.
Rodríguez, L.A., y Hernández, V.M. (2014). El pulgón Amarillo del sorgo en Tamaulipas. https://www.agrosintesis.com/el-pulgon-amarillo-del-sorgo-en-tamaulipas
Servicio Nacional de Sanidad, Inocuidad y Calidad Agroalimentaria (SENASICA). (2014). Pulgón amarillo Melanaphis sacchari (Zehntner) [Ficha Técnica, no 43]. http://www.cesavep.org/descargas/SORGO/FichaT%C3%A9cnicaNo.43Pulgonamarillo_25junio.pdf
Setokuchi, O. (1979). Damage to forage sorghum by Longiunguis sacchari (Zennther) (Aphididae). Proceeding of the Association of Plant Protection of Kyushu, 22, 139-141.
Snowden, J.D. (1955). The wild fodder Sorghums of sect Eu – Sorghum. Journal of the Linnean Society of London, 55, 191-260. https://doi.org/10.1111/j.1095-8339.1955.tb00011.x
Statistical Analysis System (SAS). (2002). SAS/ETS 9 User's Guide, Volumes 1 and 2. SAS Institute Inc.
Suárez Martínez, M. M., y Zeledón Altamirano, J. L. (2003). Uso eficiente del nitrógeno por cuatro variedades de sorgo granífero (Sorghum bicolor (L) Moench) en el municipio de San Ramón, Matagalpa [Tesis de pregrado, Universidad Nacional Agraria]. Repositorio Institucional UNA. https://repositorio.una.edu.ni/1869/1/tnf04s939.pdf
Tarwotjo, U., Rahadian, R., y Hadi, M. (2019). Abundance and diversity of insects on apple water tree during fruit season using different colours and different height placement of sticky trap. Journal of Physics: Conference Series, 1217, 1-5. https://www.doi.org/10.1088/1742-6596/1217/1/012140
Voegtlin, D., Sanchéz, M. V., Saborío, G., y Rivera, C. (2003). Guía de los áfidos de Costa Rica. Revista de Biología Tropical. International Journal of Tropical Biology and Conservation, 51(2), 1-214. https://revistas.ucr.ac.cr/index.php/rbt/issue/view/2242
Notas de autor