



Ciencias
Degradación microbiana de residuos de plaguicidas en dispositivos de biorremediación de tipo cama biológica
Microbial degradation of pesticide residues in bioremediation devices type biological bed
Revista Torreón Universitario
Universidad Nacional Autónoma de Nicaragua-Managua, Nicaragua
ISSN: 2410-5708
ISSN-e: 2313-7215
Periodicidad: Cuatrimestral
vol. 10, núm. 29, 2021
Recepción: 14 Julio 2020
Aprobación: 22 Junio 2021
Financiamiento
Fuente: Fondos para Proyectos de Investigación (FPI) de la UNAN-Managua bajo el número de proyecto 17201604
Beneficiario: Lic. Mariano Guerrero y MSc. Josseth Díaz
Descripción del financiamiento: Este proyecto de investigación fue financiado gracias a los fondos para Proyectos de Investigación (FPI) de la UNAN -Managua, bajo el número de proyecto 17201604

Resumen:
El manejo inadecuado de residuos de agroquímicos en sitios de producción agrícola implica un riesgo potencial de contaminación de las aguas superficiales y subterráneas. En estos lugares existen fuentes puntuales de contaminación que, por lixiviación o escorrentía depositan contaminantes en los cuerpos de agua aledaños a las zonas de cultivo. Para reducir este riesgo en algunas zonas se utilizan camas biológicas, esta es una matriz biológicamente activa que retiene y acelera la degradación de plaguicidas por medio de hongos ligninolíticos que se desarrollan en el material lignocelulósico que compone la cama biológica. En este estudio se evaluó la capacidad de dos sustratos biológicos para degradar y retener cipermetrina, uno elaborado con paja de sorgo y otro utilizando cascara de coco como material lignocelulósico, los experimentos realizados reflejan que el sustrato elaborado a base de paja de sorgo tiene una mayor eficiencia en cuanto a retención y degradación de cipermetrina logrando retener en promedio del 37 % de la mezcla agregada y se estimó una degradación del 90 % de la cipermetrina en un periodo de treinta días.
Palabras clave: Sustrato biológico, cipermetrina, degradación, contaminación puntual, hongos ligninolíticos.
Abstract:
The improper handling of agrochemical residues at agricultural production sites implies a potential risk of contamination of surface and groundwater. In these places there are specific sources of pollution that, by leaching or runoff, deposit contaminants in the bodies of water adjacent to the cultivation areas. To reduce this risk in some areas biological beds are used, this is a biologically active matrix that retains and accelerates the degradation process of pesticides through ligninolytic fungi that develop in the lignocellulosic material that makes up the biological bed. In this study the ability of two biological substrates to degrade and retain cypermethrin, one made with sorghum straw and the other using coconut husk as lignocellulosic material, were evaluated, the experiments carried out reflect that the substrate made from sorghum straw has a higher efficiency in terms of retention and degradation of cypermethrin achieving an average retention of 37% of the aggregate mixture and a degradation of 90% of cypermethrin was estimated over a period of thirty days.
Keywords: Biological substrate, cypermethrin, degradation, point contamination, ligninolytic fungi.
1. Introducción
El manejo inadecuado de los pesticidas puede contaminar los ecosistemas especialmente las aguas subterráneas y superficiales. Diversos estudios han demostrado que las fuentes puntuales son las que más contribuyen a la contaminación (Castillo, Torstensson, & Stenström, 2008). Un ejemplo de fuente puntual de contaminación es el sitio llenado y lavado de los equipos de aspersión. La frecuencia y el uso generalizado de sustancias químicas hechas por el hombre han llevado a un esfuerzo notable para implementar nuevas tecnologías para reducir o eliminar estos contaminantes del medio ambiente (Meleiro, Zelayrán, Consiglio, & Nitschke, 2011)
Una alternativa para reducir estos impactos es el uso de camas biológicas o biocamas en los sitios de preparación de mezclas de plaguicidas, esta es una construcción sencilla y económica diseñada para colectar y degradar derrames de plaguicidas. El propósito es que el manejo de pesticidas durante el llenado y lavado de los equipos de aspersión y embaces de plaguicidas sea hecho encima de la cama biológica de manera que si ocurren derrames accidentales los pesticidas puedan ser retenidos y degradados en la biocama. (Castillo, Torstensson, & Stenström, 2008).
El destino de los plaguicidas en el medio ambiente se ve afectado por la actividad microbiana, algunos de estos son fácilmente degradados por microorganismos (Aislabie & Lloyd-Jones, 1995), La degradación de estos en una cama biológica se logra gracias a la actividad microbiana que proporciona el sustrato biológico al estimular el crecimiento de hongos de pudrición blanca con capacidad de degradar lignina a través de la formación de enzimas ligninolíticas, como las peroxidasas y las lacasas (actividad fenoloxidasa), las cuales han demostrado también ser eficientes en la degradación de pesticidas (Proyecto D09R1006, 2013).
La cipermetrina y su metabolito ácido 3-fenoxibenzoico (PBA) han ejercido efectos biológicos adversos en el medio ambiente; por lo tanto, es de vital importancia desarrollar diferentes métodos para mejorar su degradación (XIE, ZHOU, WANG, & CHEN, 2008). En este estudio se estimó la capacidad de tres sustratos biológicos para degradar y retener cipermetrina. Se realizaron experimentos a escala de laboratorio y escala piloto con el fin de establecer cuál de ellos podría utilizarse como alternativa para mejorar el manejo de los residuos de plaguicidas en la preparación de mezcla, lavado de equipos de aspersión y embaces de cipermetrina, utilizado frecuentemente por agricultores de diferentes regiones de Nicaragua para controlar plagas de insectos.
En este estudio se evalúa la capacidad de un sustrato biológico rico en lignina para degradar cipermetrina, y fue financiado gracias a los fondos para proyectos de Investigación (FPI) de la UNAN-Managua, bajo el número de proyecto 17201604.
2. Metodología
Los plaguicidas (herbicidas, fungicidas, insecticidas) son ampliamente utilizados en la agricultura y la industria en todo el mundo. Más del 55% de la tierra usada para la producción agrícola en países en vías de desarrollo usa cerca del 26% del total de plaguicidas producidos en el mundo (Mendoza, Perea, Salvador, Morales, & Pérez, 2011). Esto es un indicativo de que, en las zonas agrícolas, sobre todo donde existen sistemas de cultivo no tecnificado puede haber un uso excesivo de agroquímicos.
Cipermetrina es un plaguicida del tipo insecticida utilizado ampliamente en el control de plagas de insectos y es utilizado rutinariamente a nivel agrícola, para el control de plagas transfronterizas y en ocasiones a nivel domiciliar. Razón por la cual se decidió utilizar este producto para realizar los ensayos La cipermetrina se adsorbe muy fuertemente en las partículas del suelo, especialmente en suelos que contienen grandes cantidades de arcilla o materia orgánica. (World Health Organization, 1989)
Para tratar de gestionar los residuos de agroquímicos se re realizaron experimentos a escala piloto para evaluar la capacidad de dos sustratos biológicos (Biomezcla) para retener una mezcla de cipermetrina preparada a una concentración 5 veces mayor (1000 mg/l) que la recomendad por el fabricante (200 mg/l). Luego se seleccionó el sustrato que presentó mejor retención y se estimó la taza de degradación de cipermetrina en experimentos a escala de laboratorio. Este experimento se realizó con concentraciones de cipermetrina elevadas ya que se asume que la biomezcla será utilizada para manejar residuos de lavado de embaces vacíos, equipos de aspersión y preparación de mezcla de cipermetrina.
2.1. Componentes y preparación de la biomezcla
Los sustratos evaluados en los experimentos fueron preparados a base de suelo, gallinaza y un material orgánico con alto contenido de lignina, este material orgánico fue la variante en los experimentos, utilizándose cascara de coco y paja de sorgo
Suelo: el suelo corresponde a un 25 % de la mezcla, y se extrae de los 20 primeros centímetros de profundidad, sin incluir la capa vegetal. El suelo aporta diversos microorganismos a la mezcla biológica, los que participan activamente en la degradación de los plaguicidas. Así mismo el suelo tiene gran capacidad de retención de los plaguicidas, dependiendo de sus características como pH y contenido de materia orgánica (Aparicio et al., 2015)
Gallinaza: En el caso de la gallinaza utilizada como composta, es decir, como abono orgánico, es necesario fermentar el excremento de las gallinas para transformar los químicos que contiene, como el fósforo, potasio, el nitrógeno y el carbono. Este conforma el 25 % de la biomezcla y aporta los nutrientes necesarios para el crecimiento de los microorganismos descomponedores de lignina.
Material orgánico: Es un material con alto contenido de lignina que se obtiene en el campo principalmente como residuos de cosecha. Para este experimento se utilizó cascara de coco y paja de sorgo, el cual contiene un 18 % de lignina (Prinsen, 2013). Estos son componentes muy importantes de la biomezcla ya que permiten o favorecen el desarrollo de muchos microorganismos, especialmente de hongos de pudrición blanca los cuales presentan elevada capacidad para degradar plaguicidas. Este componente forma el 50 % del sustrato biológico.
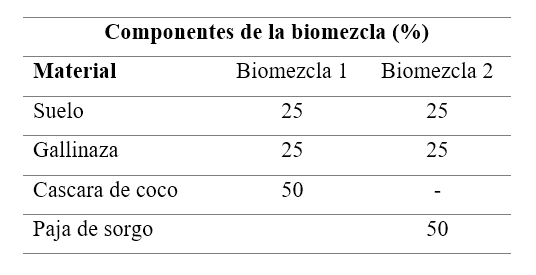
La biomezcla se preparó a las porciones descritas en la tabla 1. Cada uno de los materiales orgánicos fueron triturados y homogenizados con el resto de los componentes, y se agrega agua hasta obtener un porcentaje de humedad de aproximadamente entre el 50 % y 60 % y se deja estabilizar y madurar la biomezcla entre un periodo de 2 meses. El suelo y la gallinaza utilizada en todos los experimentos se colectó de un mismo sitio y se homogenizo de tal manera que las proporciones y el tipo de este material fuese el mismo en todos los experimentos.
2.2. Retención de la mezcla de cipermetrina
Mediante experimentos realizados a escala piloto se estimó la capacidad de retención de cipermetrina de las biomezclas elaboradas a base de cascara de coco y paja de sorgo, cada uno de estos experimentos se realizó por duplicado para identificar las variaciones en los resultados.
En un recipiente plástico se depositó un volumen aproximado de 20,00 dm3 de biomezcla, través de esta se filtraron 10,00 litros de mezcla de cipermetrina en periodo de 24 horas con un flujo de salida aproximado de 14,00 ml/min. Esta etapa se realizó durante 5 días de manera continua para evaluar la saturación del sustrato. Se colecto una alícuota de aproximadamente 100,00 ml del filtrada obtenido para su posterior análisis en el laboratorio.
2.3. Degradación de la cipermetrina
Este experimento se realizó a escala de laboratorio. Se evaluó la degradación de cipermetrina en la mezcla biológica elaborada a base de paja de sorgo durante un período de 30 días (0, 5, 10, 15, 20, 25, 30 días) se prepararon 14 muestras con aproximadamente 20,00 g de biomezcla utilizando paja de sorgo como material orgánico y enriquecidas con 2,00 ml de la mezcla de 1000,00 mg/l para obtener una concentración de cipermetrina en el sustrato de 100,00 mg/kg. El análisis se realizó por duplicado y las muestras a procesar en cada periodo de tiempo se seleccionaron del lote de muestras al azar.
2.4. Procesamiento de muestras
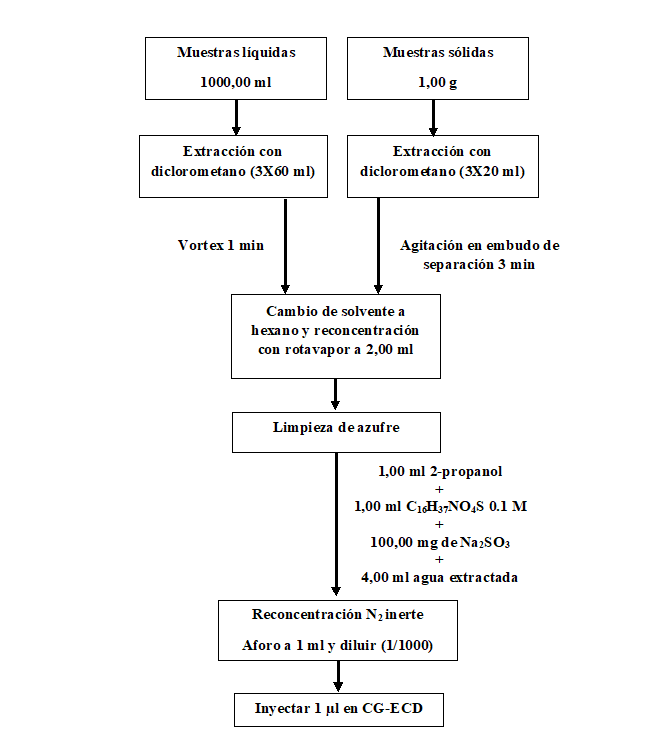
Las muestras líquidas y sólidas fueron extractadas con diclorometano de acuerdo al procedimiento descrito por el laboratorio de contaminantes orgánicos del CIRA /UNAN-Managua para cada una de estas matrices.
En las muestras líquidas se midió una alícuota de 1,00 ml del total colectado, se depositó en un balón de 1000,00 ml y se aforó hasta la marca de enrace. El contenido total del balón se extractó con 180,00 ml de diclorometano (3 x 60,00 ml), se filtró el extracto orgánico con sulfato de sodio anhídrido y se depositó en un balón de 250,00 ml para luego ser reconcentrado con un rotaevaporador (BÜCHI RE 121) a un volumen aproximado de 3,00 ml, con cambio de solvente a hexano. El contenido del balón se trasladó a un tubo de 12,00 ml, se reconcentró con una corriente de N2 inerte a un volumen aproximado de 2,00 ml para luego realizar limpieza de azufre con 1,00 ml de 2 propanol + 1,00 ml TBA 0.1 M (tetrabutilamonio hidrogeno sulfato) saturado con sulfito de sodio + 100,00 mg de sulfito de sodio + 4,00 ml de agua extractada. El extracto orgánico obtenido se aforó a 1,00 ml y se inyectó 1 µl en el cromatógrafo de gases con detector de captura de electrones (GC-ECD).
Para las muestras sólidas se pesó un total de 20,00 g y se extractó con 60,00 ml de diclorometano (3 x 20,00 ml) por agitación vortex (vortex mixer Heidolph REAX 2000). El extracto orgánico se filtró con sulfato de sodio anhídrido y se depositó en un balón de 250,00 ml para luego ser reconcentrado con un rotaevaporador (BÜCHI RE 121) a un volumen aproximado de 3,00 ml, con cambio de solvente a hexano. El contenido del balón se trasladó a un tubo de 12,00 ml, se reconcentró con una corriente de N2 inerte a un volumen aproximado de 2,00 ml para luego realizar limpieza de azufre. El extracto orgánico obtenido se aforó a 1,00 ml y se inyectó 1 µl en el cromatógrafo de gases con detector de captura de electrones (GC-ECD).
2.5. Condiciones instrumentales para el análisis de muestras
Los extractos de las muestras se inyectaron en un cromatógrafo de gases con detector de captura de electrones (Perkin Elmer Clarus 500). columna Agilent DB-5 de (30 m x 0.32 mm) 0.25 micrómetros grosor de la película de la fase estacionaria. Programación de horno 100 °C hold time 1 minuto, 4 °C/min hasta 200 °C, 3 °C/min hasta 230 °C, 15 °C/min hasta 280 °C, hold time 5 minutos; Temperatura de inyector 250 °C; Volumen de inyección 1 µl; Gas portador hidrógeno con flujo de 2 ml/min; Temperatura de detector 350 °C; Gas de respaldo nitrógeno con flujo de 28 ml/min; rango 1 y atenuación -4.
3. Resultados
Los sustratos biológicos elaborados a base de paja de sorgo (Biomezcla 2) y cascara de coco (Biomezcla 1) reflejan resultados de retención en promedio durante los 5 días de experimento fueron de 86.39 % y 66.07% respectivamente, sin embargo, el experimento realizado con cascara de coco refleja un mayor coeficiente de variación y una disminución de la remoción del 61.78 % al comparar el primero y el último día, mientras que con paja de sorgo la disminución fue del 28.34 %.
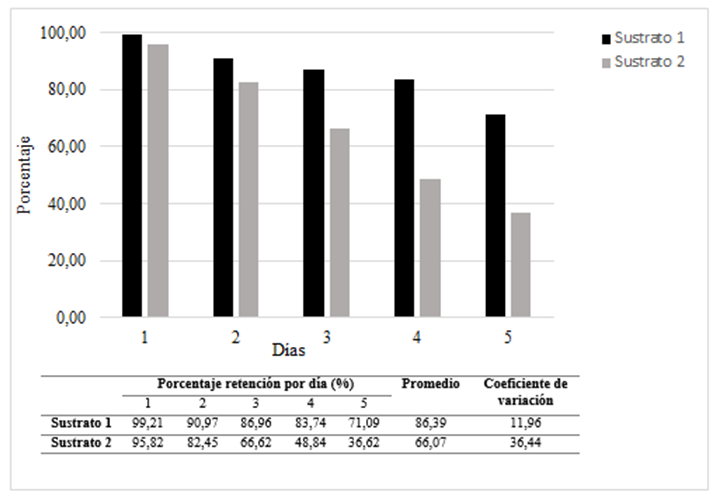
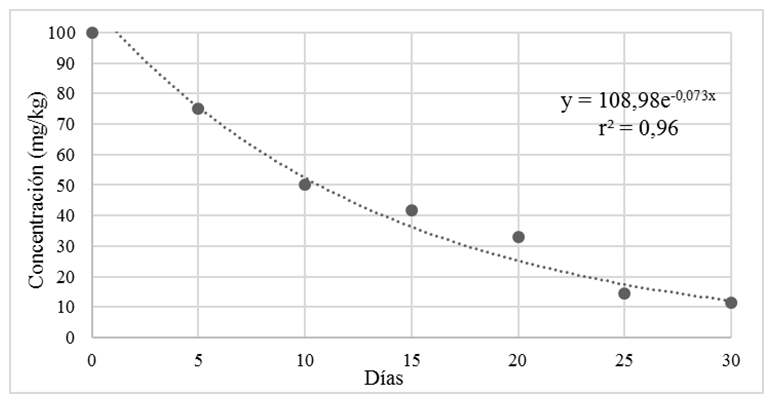
Estos resultados (figura 2) reflejan mayor eficiencia en la retención de cipermetrina para los experimentos utilizando paja de sorgo como sustrato biológico, por tal razón se decidió utilizar este material para evaluar la degradación de cipermetrina utilizando este material para aportar lignina a la biomezcla. La concentración inicial de cipermetrina en la biomezcla fue aproximadamente de 100,00 mg/kg al finalizar los 30 días que duró el experimento se obtuvo una concentración final de cipermetrina promedio de 11,35 mg/kg.
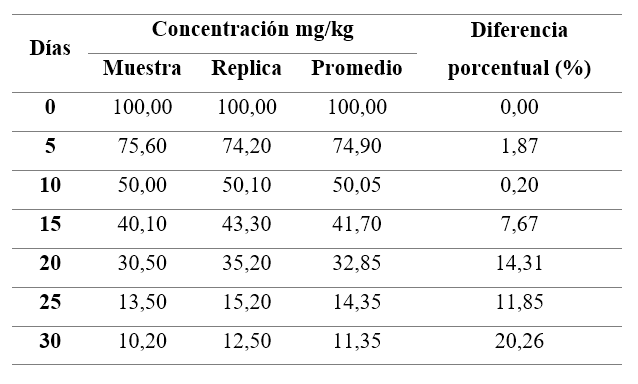
Al evaluar la degradación de la cipermetrina en el experimento elaborado a base de paja de sorgo (Figura 3) se determinó que el 90 % de la cipermetrina presente en la biomezcla se degrada en un periodo de 30 días. Los datos obtenidos presentan una distribución exponencial con un coeficiente de determinación (r2) de 0,96.
4. Discusión
La biomezcla preparada con paja de sorgo como material orgánico para aportar lignina al sustrato presenta mejores resultados de retención de cipermetrina, lográndose retener un 86 % de la cipermetrina agregada al sustrato durante los 5 días que duró el experimento, esto demuestra que el sustrato es eficiente para retener derrames de cipermetrina y manejar los residuos de lavado y preparación de mezclas.
Se determinó que el 90 % de la cipermetrina agregada a las muestras se degradó en un periodo de 30 días y a pesar que se vertieron altos volúmenes de líquidos a concentraciones de mezcla por encima de lo que recomienda el fabricante para la fumigación de cultivos, el sustrato elaborado a base de paja de sorgo permitió acelerar el proceso de degradación de la cipermetrina, no obstante, la simple remoción de la molécula del pesticida original no indica que el tratamiento es ecológico debido a la formación de metabolitos de alta toxicidad que son difíciles de identificar y cuantificar (Rodríguez, Castro, & Lizano, 2018).
Para determinar si existe algún tipo de metabolito de degradación en el proceso de degradación se debe ampliar el estudio e identificar estas moléculas, más sin embargo la función de la cama biológica para la retención de derrames logra evitar el arrastre o la lixiviación de residuos de plaguicidas hacia algún cuerpo de agua o el acuífero.
5. Conclusiones
Los experimentos realizados en las pruebas de retención y degradación reflejan que la mezcla biológica elaborada a base de paja de sorgo es efectiva para el manejo de residuos de cipermetrina y podría ser utilizada para verter los residuos líquidos procedentes del lavado de equipos de aspersión y enjuague de recipientes vacíos de plaguicidas y de esta manera acelerar el proceso de degradación natural de este plaguicida. Es recomendable evaluar la eficiencia del sustrato en campo y demostrar la efectividad para retener y degradar plaguicidas por un periodo más prolongado, a condiciones de trabajo real y así identificar qué factores podrían influir en la eficiencia del sustrato, de igual manera es importante validar la metodológica con otras moléculas de plaguicidas y determinar si pudiesen existir variaciones en la degradación al usarlo con mezclas de plaguicidas y sobre todo cuando se agrega algún tipo de funguicida en la mezcla.
Agradecimientos
Este estudio fue financiado gracias a los fondos para proyectos de Investigación (FPI) de la UNAN-Managua, bajo el número de proyecto 17201604
Bibliografía
Aislabie, J., & Lloyd-Jones, G. (1955). A review of bacterial degradation of pesticides. Australian journal of soil research, 925-942.
Aparicio, V., De Gerónimo, E., Hernández, K., Pérez, D., Portocarrero, R., & Vidal, C. (2015). Los plaguicidas agregados al suelo y su destino en el ambiente. INTA.
Castillo, M., Torstensson, L., & Stenström, J. (2008). Camas Biológicas Para La Preservación Del Medio Ambiente De La Contaminación Por Pesticidas. Journal of Agricultural and Food Chemistry 56, 6206-6219.
Meleiro, A., Zelayrán, G., Consiglio, M., & Nitschke, M. (2011). Biodegradation of Pesticides. Pesticides in the Modern World – Pesticides Use and Management, 407-438
Mendoza, J., Perea, Y., Salvador, J., Morales, J., & Pérez, G. (2011). Biodegradación bacteriana de plaguicidas permetrina y cipermetrina en cultivo lote. Avances en ciencia e ingeniería, 45-55.
Prinsen, P. (2013). Caracterización química y estructural de lignina y lípidos de materiales lignocelulósicos de interés industrial (Memoria de investigación para optar al grado de doctor en ciencias químicas). Sevilla, España.
Proyecto D09R1006. (2013). Manual de construcción y operación de lechos biológicos. Universidad de La Frontera.
Rodríguez, C., Castro, V., & Lizano, V. (2018). Alternative approaches to determine the efficiency of biomixtures used for pesticide degradation in biopurification systems. En E. Dino, & R. Nallin, Toxicity and biodegradation testing (págs. 57-73)
World Health Organization. (1989). Environmental Health Criteria. Cypermethrin. Ginebra.
Xie, W.-J., Zhou, J.-M., Wang, H.-Y., & Chen, X.-Q. (2008). Effect of nitrogen on the degradation of cypermethrin and its metabolite 3-phenoxybenzoic acid in soil. Pedosphere, 638–644.

